Elektrolyse
Elektrolyse ist das Zersetzen einer stromleitenden Flüssigkeit (Elektrolyt), zum Beispiel Wasser (H2O), beim Anlegen einer Spannung. Die Moleküle der Salze, Säuren oder Laugen zerfallen im Wasser in elektrisch geladene Teilchen (Ionen). In den Elektrolyten sind die Ionen die Träger der elektrischen Ladung.
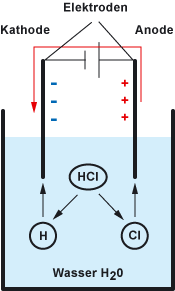
Bei dem dargestellten Versuch spielen sich folgende Vorgänge ab:
Die Chlorwasserstoff-Atome (HCl) reagieren mit den Wasser-Atomen (H2O) und zerlegen sich in elektrisch geladene Ionen. Dabei entstehen Chlor-Ionen (Cl) und Wasserstoff-Ionen (H). Die Chlor-Ionen (Cl) sind negativ geladen. Die Wasserstoff-Ionen (H) oder Hydronium-Ionen sind positiv geladen.
Durch die Spannung an den Elektroden (Anode und Kathode) wandern die Ionen an die jeweils entgegengesetzt geladene Elektrode. Die negativ geladenen Chlor-Ionen wandern zur Anode (positiv geladen) und die positiv geladenen Wasserstoff-Ionen wandern zur Kathode (negativ geladen). Es kommt dabei zu einem Stromfluss, dem Ionenstrom.
Elektrolyt
Der Elektrolyt ist eine stromleitende Flüssigkeit, die meist aus Wasser (H2O) besteht, das in der reinen Form nicht leitend ist. Erst durch Hinzufügen von Verunreinigungen wird das Wasser leitend. Das normale Wasser, das aus der Leitung kommt ist als verunreinigt anzusehen. Verunreinigt man das Wasser gezielt mit Säuren, Laugen oder Salzen, entsteht ein Elektrolyt, das für die Elektrolyse verwendet werden kann.
Anwendungen
- Galvanostegie (Galvanisierung)
- Galvanoplastik
- Elektrolytkupferherstellung (Elektronikkupfer)
- elektrolytisches Polieren
- elektrolytisches Formentgraten
- Elektrolytkondensator
- Eloxieren (Oxidschicht auf Aluminium)
Weitere verwandte Themen:
- Chemie Grundlagen
- Atome, Elektronen und Ionen
- Galvanische Elemente
- Galvanische Primärelemente
- Galvanische Sekundärelemente
- Brennstoffzelle
Lernen mit Elektronik-Kompendium.de
Noch Fragen?
Bewertung und individuelles Feedback erhalten
Elektronik-Fibel
Elektronik einfach und leicht verständlich
Die Elektronik-Fibel ist ein Buch über die Grundlagen der Elektronik, Bauelemente, Schaltungstechnik und Digitaltechnik.
Elektronik-Fibel
Elektronik einfach und leicht verständlich
Die Elektronik-Fibel ist ein Buch über die Grundlagen der Elektronik, Bauelemente, Schaltungstechnik und Digitaltechnik.
Elektronik-Set Starter Edition
Elektronik erleben mit dem Elektronik-Set Starter Edition.
Perfekt für Einsteiger und Wiedereinsteiger.
Keine Lust alleine zu experimentieren?
Dann buche einen Online-Workshop Elektronik Starter zum Elektronik-Set dazu. Unsere Online-Workshops sind praxisorientiert und bietet eine grundlegende und fundierte Einarbeitung in die Elektronik.
Das Elektronik-Set der anderen Art: Der Roboter-Bausatz VARIOBOT varikabi
Der VARIOBOT varikabi ist ideal für einen spannenden Einstieg in die Elektronik. Er kommt ohne komplexe Steuerung und Programmierung aus.




